CPR ng Dengvaxia 'permanently revoked' na
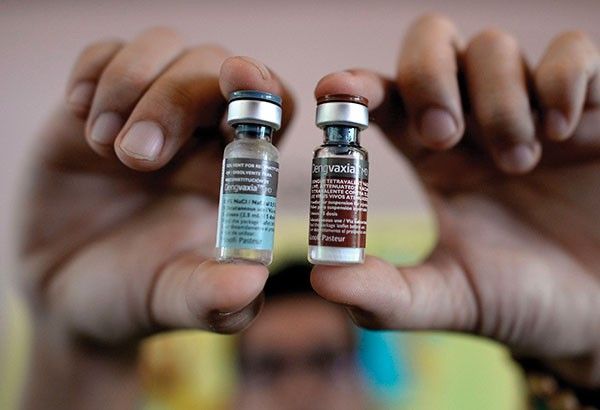
MANILA, Philippines — Tuluyan nang ni-revoke ng Food and Drug Administration ang Certificate of Product Registration ng kontrobersyal na Dengvaxia, isang bakuna kontra dengue.
Una nang sinuspinde ng FDA ang CPR nito noong ika-29 ng Disyembre taong 2017 dahil sa 'di pagsunod ng pharmacuetical firm na Sanofi Pasteur sa post-marketing requirements. Isinagawa ito dahil sa mga "adverse" reactions sa mga naturukan nito.
Ayon sa FDA, tila sadyang binalewala ng Sanofi ang mga panuntunan at regulasyon nila.
“Its brazen defiance of FDA’s directives and its continued failure to comply leaves us no other recourse but to impose the maximum penalty of revocation of the CPRs covering the Dengvaxia products,” ayon kay Nela Puno, director general ng FDA.
Pinaalalahanan din ng FDA ang Sanofi na bawal nang mag-angkat, magbenta at mag-distribute ng naturang bakuna sa bisa ng CPR revocation.
Ayon sa ahensya, kinumpirma ng Center for Drug Regulation and Research, sa pakikipagtulungan ng Task Force Dengvaxia, na hindi pa rin nagsusumite ng post-marketing authorization requirements ang Sanofi noong ika-17 ng Disyembre 2018.
Sa utos na pinirmahan ni Puno noong ika-21 ng Disyembre, iginiit ng FDA na isuko ng Sanofi ang kanilang orihinal na CPR ng dengue tetravalent (live attenuated) (Dengvaxia MD) at dengue tetravalent vaccine (live attenuated) (Dengvaxia) pagkakuha ng order.
Inatasan na rin daw ng CDRR na i-defer ang pagpro-proseso ng anumang submission at application ng Sanofi kaugnay ng Dengvaxia at Dengvaxia-MD.
Humaharap sa kontrobersiya ang Dengvaxia matapos iugnay sa pagkamatay ng ilang estudyanteng naturukan nito.
- Latest